
일러스트 McCall Sarrett
20 년 동안의 삶을 잊어 버리거나 매 5 분마다 같은 대화를 나눌 때마다 기억 장애가 일상 생활에 큰 타격을 줄 수 있습니다. 그것은 신경 퇴화의 가장 혼란스러운 측면 중 하나 일 수 있으며 치매의 주요 증상입니다.
알츠하이머 병, 또한 ~으로 알려진 AD인지 기능 장애 및 기억력 상실로 특징 지어지는 가장 흔한 형태의 치매입니다. 부검을 제외하고 현재 AD 진단을위한 공식 임상 기술은 없습니다. 그러나 알츠하이머 병 환자의 뇌 조직에는 두 가지 특징이 있습니다. 아밀로이드 베타 (ㅏ?) 플라크 (plaques) 및 신경 원 섬유 엉킴 (neurofibrillary tangles)을 포함하며, 이들 모두는 신경 퇴행의 병리학에 대한 실질적인 통찰력을 제공한다.
"신경 피질 엉킴은 타우 단백질 (tau proteins)이라고 불리는 단백질 결함으로 인해 발생합니다."
ㅏ? 결과로 나오는 단백질이다. 단백질 분해 of 아밀로이드 전구체 단백질 (APP). 이는 APP가 더 작은 조각으로 절단되며 그 중 하나가 A? 파편. APP는 분비효소라고 불리는 효소에 의해 이러한 조각으로 절단되는데, 이 효소의 주요 역할은 이러한 단백질을 절단하는 것입니다. 다양한 분비효소가 존재하지만, 알츠하이머 병리학에서 중요한 것이 하나 있는데, 바로 감마 분비효소입니다. 감마 세크레타제는 특별한 형태의 Aβ: Aβ-42, 즉 가장 독성이 강한 단백질 형태를 생성합니다. 일단 분해되면 이러한 단백질 조각은 세포 외부 공간에 모이기 시작합니다. 이러한 단백질의 독성에 대한 핵심은 특징적으로 "끈적"하여 응집체를 형성하기 시작한다는 것입니다. 이러한 응집체는 계속해서 발달하고 곧 이러한 아밀로이드 베타 플라크가 도처에 퍼져 신경 기능을 크게 손상시킵니다.
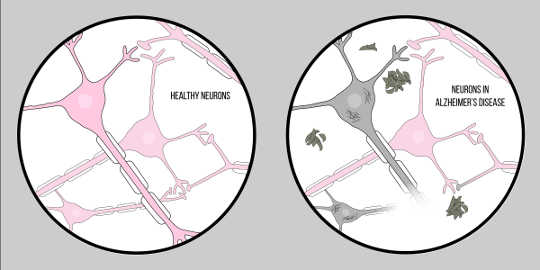 McCall Sarrett의 그림
McCall Sarrett의 그림
A의 영향은? 신경학적 기능에 대한 결과는 다음과 같습니다. 아밀로이드 가설, 알츠하이머 병의 신경 퇴화에 대한 설명을 제안하는 잘 알려진 이론.
이제, 두 번째 주요 특징 : 신경 섬유 엉킴. 신경 섬유 얽힘은 타우 단백질 (tau proteins)이라고 불리는 단백질 결함으로 발생합니다. Tau 단백질은 세포 내에서 미세 소관 (microtubules)이라고 불리는 구조물 사이의 다리 역할을합니다. 미세 소관은 세포에 모양과 구조, 특히 축삭을 제공하는 분자를지지합니다. Tau 단백질은 이러한 미세 소관이 축색 돌기에 구조를 제공 할 수 있도록 도와줍니다. 그러나, 알츠하이머 병신경 세포의 손실이 특징 인 신경 퇴행성 질환은 세포 소체 (soma)로 알려진 타우 단백질 (tau proteins)을 분리하여 축적합니다. 이것은 축삭의 퇴행을 일으키므로 뉴런이 의사 소통을하기가 훨씬 더 어렵습니다. 연결의이 어려움은 아밀로이드 베타의 효과와 유사합니다. 그러나 이러한 엉킴은 외부와 반대로 세포 내부로부터의 커뮤니케이션에 영향을 준다는 점에서 앞서 논의한 플라크와 크게 다르다는 점에 유의하는 것이 중요합니다.
"과학자들은 여전히 알츠하이머 병의 원인이되는 정확한 기전을 확신하지 못하고있다."
둘 다 매우 영향력이 있지만 A? 그리고 타우가 알츠하이머병의 병리와 관련하여 관련된 유일한 요인은 아닙니다. 연구에 따르면 아포지단백질 E(APOE)는 유전자 A만큼 영향력이 있을 수 있습니까? 단백질을 암호화하는 세 가지 주요 변종은 ApoE2, ApoE3 및 ApoE4입니다. ApoE4는 시냅스 가지치기의 감소와 상관관계가 있는 것으로 나타났으며, ApoE2는 증가를 초래합니다. 두 형태 모두 영향을 미칩니다 성상 세포 (중대한 신경 교세포 신경계 내에서), 그리고 식세포 증가 속도와 상관 관계가있다. 성상 세포별 모양의 신경 교세포는 많은 기능을 가지고 있습니다. 각각의 ApoE 변이가이 식세포 증가 비율 ApoE2에 직접적으로 영향을 미치고 ApoE4는 감소합니다. 이것은 성상 교세포가 ApoE4와 관련되었을 때 세포 주위에 떠 다니는 파편을 "제거"할 수 없을 수도 있음을 시사합니다. 따라서 이러한 플라크가 형성되면 ApoE4 유전자형은 퇴화에 기여하는 이러한 응집체의 제거를 방지 할 수 있습니다.
아밀로이드 베타, 타우 및 다양한 유전자가 모두 작용하여 세포간에 주요 커뮤니케이션 문제가 발생합니다. 이는 본질적으로 우리가 알츠하이머 병으로 알고있는 질환입니다. 이러한 신경 퇴행은 학습과 기억과 관련된 두뇌 영역에서 가장 흔하지만 결국 뇌 전체에 퍼집니다. 이러한 소통의 결여로 시냅스의 상실과 결국 뇌 물질의 감소가 초래됩니다. 따라서 뇌 조직이 감소한 것을 보는 것이 정상입니다. MRI자기 공명 영상 (Algorithmic imaging)은 병이 진행됨에 따라 스트레스를 보는 기술이며, 알츠하이머가 말 그대로 뇌를 수축 시킨다는 것을 보여줍니다. 학습과 기억에 관한 우리의 현재 모델은 시냅스가 이러한 과정에서 핵심적인 역할을한다는 것을 밝힙니다.이 병리가 기억 상실과 같은 AD의 주요 증상과 어떻게 관련이 있는지에 대한 가능한 설명을 제공합니다.
과학자들은 여전히 알츠하이머 병의 원인이되는 정확한 기전을 확신하지 못하고있다. 많은 혁신적인 방법이 뇌척수액 (CSF) 바이오 마커 인이 병리학 적 포인트에 대한 더 많은 지식을 얻기 위해 연구되었습니다.
A급? 타우는 뇌척수액을 수집하는 요추 천자라는 절차를 통해 CSF에서 측정될 수 있습니다. 타우 수준은 증가하고 A 수준은 감소합니까? 알츠하이머병 환자에게서 나타난다. 이것은 A? 뇌에 축적되어 뇌척수액 농도가 감소합니다. 이 데이터는 미래에 의사와 과학자들이 CSF의 단백질 수준을 검사하여 환자의 인지 상태를 예측할 수 있음을 시사합니다.
현재 알츠하이머 병에 대한 확실한 치료법은 없습니다. 그러나 관련된 병리학 적 단백질, 관련 유전자 및 진행중인 과학 연구에 대한 지식의 증가는 장차 효과적인 치료법에 대한 희망을 제공합니다.
알츠하이머 병 치료를 위해 의약품이 필요한 돌파구는 무엇입니까? 의견을 통해 알려주십시오!
이 문서는 원래의 등장 뉴런을 아는 것?
저자에 관하여
Khayla Black은 New York University Shanghai의 한 신입생으로 인공 지능이 집중된 Data Science의 미성년자와 함께 신경 과학 분야의 전공을 선보일 계획입니다. 미래에는 MD / PhD를 얻고 학습과 기억의 분자 적 측면을 연구하는 신경 과학자가되기를 희망합니다. 여가 시간에 Khayla는 IYNA 내의 MYELIN 이니셔티브 및 신경 과학 관련 자료를 읽는 것을 즐깁니다. 신경 과학을 공부하는 것 외에, 그녀는 달리기, 지역 초등학교에서의 가르치기, 수학 문제 해결, 엄청난 양의 커피 마시기 등을 즐깁니다.
관련 서적
at 이너셀프 마켓과 아마존
참고자료
Lacor, PN, Buniel, MC, Furlow, PW, Clemente, AS, Velasco, PT, Wood, M., . . . 클라인, WL (2007년 24월 XNUMX일). ㅏ? 올리고머로 인한 수차 시냅스 구성, 모양 및 밀도는 알츠하이머 병의 연결성 상실에 대한 분자 기반을 제공합니다. 에서 가져온 http://www.jneurosci.org/content/27/4/796
머피, MP, & 르빈, H. (2010). 알츠하이머병과 β-아밀로이드 펩티드. 알츠하이머병 저널: JAD, 19(1), 311. http://doi.org/10.3233/JAD-2010-1221
O'Brien, RJ, & Wong, PC (2011). 아밀로이드 전구체 단백질 처리 및 알츠하이머 병. 신경 과학 연간 검토, 34, 185-204. http://doi.org/10.1146/annurev-neuro-061010-113613
Chung, W.-S., Verghese, PB, Chakraborty, C., Joung, J., Hyman, BT, Ulrich, JD, ... Barres, BA (2016). APOE의 비율 조절에있어 새로운 대립 유전자 의존 역할 시냅스신호가 전달 된 뉴런 사이의 연결 ... 성상 세포에 의한 가지 치기. 미국 국립 과학원 학술회 논문집, 113(36), 10186-10191. http://doi.org/10.1073/pnas.1609896113
Zetterberg, H. (2009년 19월 XNUMX일). 아밀로이드? 알츠하이머병의 바이오마커로서의 APP. 검색 위치 https://www.sciencedirect.com/science/article/pii/S0531556509001594?via=ihub























